Aurobindo Pharma Ltd從美國食品和藥物管理局(US FDA)收到了自願採取行動(VAI)的暗示,將其懸垂部分解除了其中一部分。但這雖然令人欣慰,但該公司必須快速跟蹤在美國的新產品發布,結束對Sandoz的收購併必須從美國監管機構處清除其他工廠。
不過,華爾街對美國FDA的第4單元的VAI感到非常驚訝,因為某些觀察本質上要求很高。美國食品和藥物管理局還一直在加強製藥行業的監管行動,最近這影響了許多印度製藥商。最近,Aurobindo還為其其他一些設施收到了官方的行動指示和警告信,因此,這確實受到歡迎。
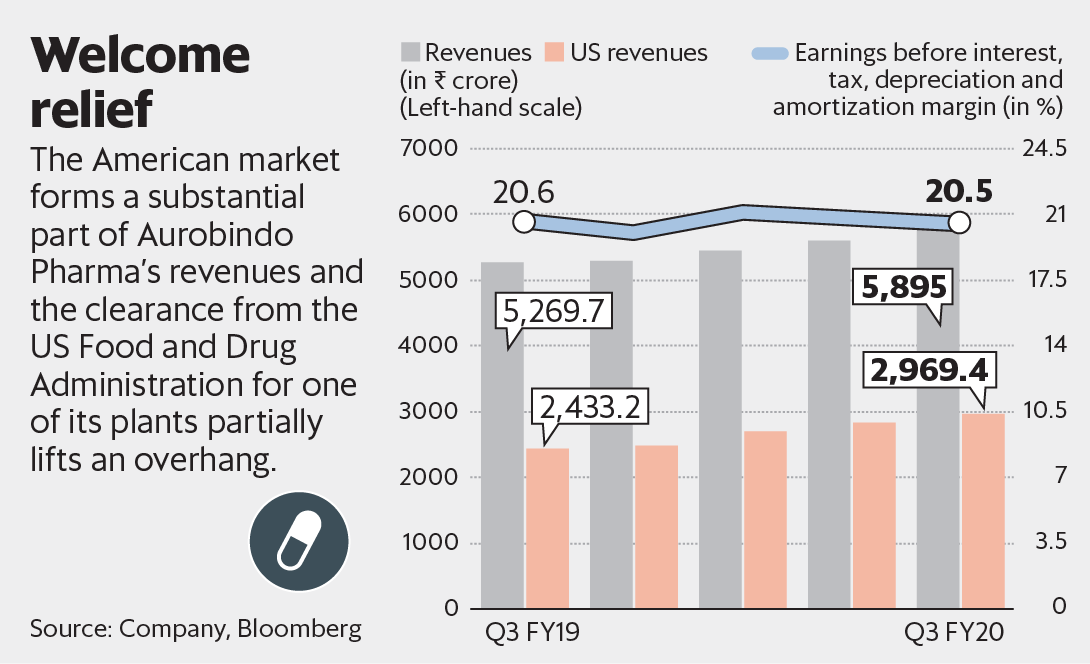
但是,最近的VAI顯示,Aurobindo暫時不必擔心此關鍵的IV單元工廠的新葯上市。請注意,IV單元是該公司的重要無菌設施,約佔其在美國待審批的簡短新葯申請(ANDA)的近三分之一。因此,這種植物對於未來的增長至關重要。實際上,該工廠已經產生了很大一部分收入。
 圖片:Naveen Kumar Saini / Mint
圖片:Naveen Kumar Saini / Mint
「我們的估計已經假定有第四單元的許可;現在,清算使我們在2021/22財年分別對無菌業務的收入預測分別為2.8億美元和3.43億美元,」他說。
儘管如此,投資者現在正在展望該公司以多快的速度完成對Sandoz的收購,Sandoz有許多關鍵產品有望產生可觀的收入。
但是,Sandoz的一些主要分銷協議有望終止,這可能會阻礙收入增長。不過,Aurobindo仍可以使用Sandoz的三個設施,這有助於加強產品組合以及成本協同效應。
但是,美國FDA仍在對其應進行檢查的其他一些工廠進行檢修。 「美國食品藥品管理局將從2月24日開始在第10單元進行檢查,並於4月某個時候開始在Eugia單元進行檢查。兩者總共容納62個待審核的ANDA,占待審核批准的40%。這些部門將是未來2-3年的主要增長動力。 Sandoz監管部門的批準是另一個可監控的關鍵。」 BoB Capital Markets Ltd的分析師在一份報告中說。
不過,Aurobindo股票在過去兩天內上漲了19%,這使其在現階段的價格相當昂貴。畢竟,一些增長挑戰仍然存在。此外,擴大其新設施和產品批准的步伐將是未來庫存前景的關鍵。
話題
Aurobindo Pharma美國FDA





